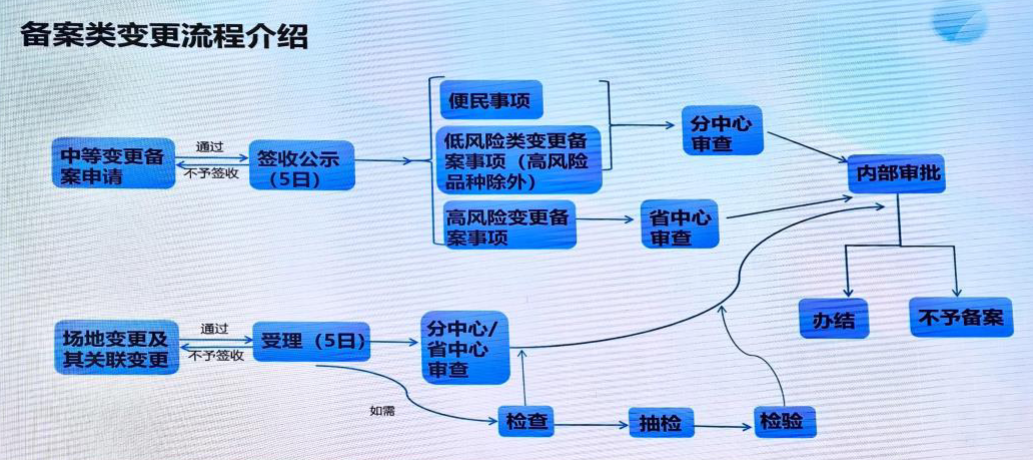
问题:按照法规说法,备案不属于行政审批,备案提交即完成。比如涉及到物料的变更。备案后什么时间点可以实施?是提交备案受理后,还是取得备案批准后?如果在提交备案后开始生产,控制不放行,在取得审批后放行,会有什么样的市场影响。
法规如下:
- 药品上市后变更管理办法(试行)
第四条 持有人是药品上市后变更管理的责任主体,应当按照药品监管法律法规和药品生产质量管理规范等有关要求建立药品上市后变更控制体系;根据国家药品监督管理局有关技术指导原则和国际人用药注册协调组织(ICH)有关技术指导原则制定实施持有人内部变更分类原则、变更事项清单、工作程序和风险管理要求,结合产品特点,经充分研究、评估和必要的验证后确定变更管理类别。
第五条 注册变更管理类别根据法律法规要求和变更对药品安全、有效和质量可控性可能产生影响的风险程度,分为审批类变更、备案类变更和报告类变更,分别按照《药品注册管理办法》《药品生产监督管理办法》的有关规定经批准、备案后实施或报告。
第四十三条 药品上市许可持有人应当按照药品生产质量管理规范的要求对生产工艺变更进行管理和控制,并根据核准的生产工艺制定工艺规程。生产工艺变更应当开展研究,并依法取得批准、备案或者进行报告,接受药品监督管理部门的监督检查。
3. <药品注册管理办法>
第七十九条 以下变更,持有人应当在变更实施前,报所在地省、自治区、直辖市药品监督管理部门备案:
(一)药品生产过程中的中等变更;
(二)药品包装标签内容的变更;
(三)药品分包装;
(四)国家药品监督管理局规定需要备案的其他变更。
境外生产药品发生上述变更的,应当在变更实施前报药品审评中心备案。
药品分包装备案的程序和要求,由药品审评中心制定发布。
4.《药品上市后变更管理办法(试行)》政策解读
二十五、备案的法律意义是什么?
根据我国法律规定和国务院规定,备案不属于行政许可,不存在许可类备案,《办法》规定的备案均为告知性备案,由持有人对备案事项负主体责任。
二十六、备案时限是多少?
备案不是行政许可,持有人按照备案资料要求提交资料进行备案,提交备案资料后即完成备案。
这{{threadTextType}}正{{isAdminText}}
为帮助审核人员更快处理,请填写举报原因:
为帮助审核人员更快处理,请填写举报原因: